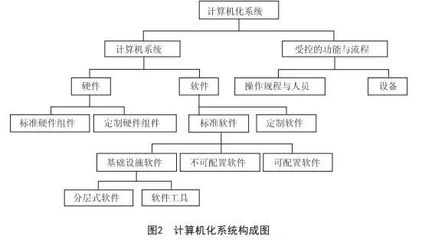
在药品生产质量管理规范(GMP)日益严格的全球背景下,计算机化系统验证(CSV)已成为确保制药企业生产数据完整性、产品质量与合规性的核心环节。GAMP5(良好自动化生产实践指南第5版)作为国际公认的计算机化系统生命周期管理框架,为我国制药企业提供了系统化、风险导向的验证方法论。本文旨在探讨基于GAMP5的计算机化系统验证在我国制药企业的应用现状、挑战及优化路径,以促进产业升级与合规水平提升。
一、GAMP5框架的核心原则与验证流程
GAMP5框架强调“基于风险、生命周期管理、供应商参与”三大支柱,将计算机化系统验证融入从概念到退役的全过程。其核心流程包括:
- 分类与风险评估:根据系统复杂性与影响程度(如直接影响产品质量的GxP系统),确定验证深度与范围。
- 生命周期管理:涵盖用户需求说明(URS)、设计确认(DQ)、安装确认(IQ)、运行确认(OQ)、性能确认(PQ)等阶段,确保系统始终处于受控状态。
- 供应商管理:利用供应商评估与文档支持,降低自开发系统的验证负担。
二、我国制药企业计算机化系统验证的应用现状
随着《药品生产质量管理规范(2010年修订)》及附录《计算机化系统》的发布,我国制药企业已普遍启动CSV实践,但应用水平参差不齐:
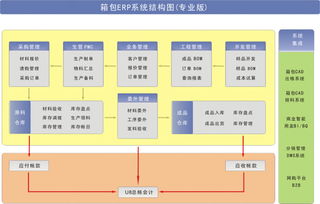
- 优势领域:大型跨国或领先本土企业在ERP、MES、LIMS等核心系统验证中,已逐步采用GAMP5框架,形成标准化流程,并借助自动化工具提升效率。
- 普遍挑战:中小型企业常面临资源有限、专业人才缺乏、验证文档形式化等问题。部分企业将验证视为“一次性合规任务”,忽视持续监控与变更控制,导致系统后期运维风险升高。
- 技术痛点:对云计算、物联网等新兴技术的验证经验不足,传统验证方法难以完全适应敏捷开发与持续交付模式。
三、基于GAMP5的优化实践路径
为提升验证效能与合规水平,我国制药企业可聚焦以下方向:
- 建立风险导向的验证策略:依据系统GxP影响分级,差异化配置验证资源。例如,对高风险的工艺控制系统实施全生命周期验证,而对低风险的办公软件采用简化流程。
- 强化供应商协作与文档复用:优先选择符合GAMP5标准的供应商,利用供应商提供的验证包(如设计文档、测试案例)减少重复工作,同时通过审计确保其质量体系可靠性。
- 推动验证流程自动化与数字化:引入专用CSV管理软件或集成式平台,实现需求追踪、测试执行、缺陷管理、文档生成的自动化,降低人为错误并提升可追溯性。
- 培育专业人才与合规文化:通过内训、行业交流及第三方服务合作,构建既懂GMP又熟悉IT技术的复合型团队,并将验证意识融入日常运维与变更管理。
- 适应新技术与敏捷模式:针对云部署、AI分析等系统,在GAMP5灵活框架下探索“迭代验证”与“持续验证”方法,结合敏捷开发周期嵌入验证活动,确保合规性与创新平衡。
四、结论与展望
GAMP5框架为我国制药企业计算机化系统验证提供了科学且适应性强的指南。随着监管要求的细化与工业4.0技术的渗透,企业需进一步将验证从“合规驱动”转向“质量与效率驱动”,通过标准化、自动化与智能化手段,构建稳健的计算机化系统治理体系。这不仅有助于通过国内外GMP审计,更能为药品全生命周期数据可靠性与患者安全奠定坚实基础,最终推动我国制药行业的高质量发展。